Những điều cần biết về liên kết hóa học của năm học lớp 10
Liên kết hóa học là một trong những kiến thức quan trọng trương chươn trình Hóa Học lớp 10, Nó quyết định tới tính chất của các chất hóa học trong phản ứng. Hãy cùng gia sư Hà Nội tìm hiểu nội dung quan trọng này qua bài viết dưới đây nhé.
Liên kết hóa học và các khái niệm liên quan
Liên kết hóa học là gì? Nó là lực giữ cho các nguyên tử, nguyên tố nối kết với nhau trong các phân tử hay tinh thể. Từ khi được nghiên cứu tới nay, đã có vô vàn các học thuyết khác nhau viết về chủ đề nay, có thể kể ra như thuyết liên kết hóa trị và khái niệm số oxi hóa nhằm dự đoán cấu trúc và thành phần phân tử; thuyết vật lý cổ điển về liên kết điện tích để dự đoán các cấu trúc ion…Điểm chung của các thuyết trên tập trung nói về:
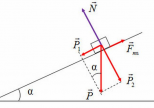
Độ dài liên kết: khoảng cách giữa hai hạt nhân của các nguyên tử tương tác với nhau.
Góc hóa trị: góc tạo thành bởi 2 đoạn thẳng nối hạt nhân nguyên tử trung tâm với 2 hạt nhân nguyên tử liên kết.
Năng lượng liên kết: năng lượng được giải phóng ra khi tạo thành liên kết đó từ các nguyên tử.
Bậc liên kết: Là số liên kết tạo thành giữa 2 nguyên tử tương tác trực tiếp với nhau.
Ngoài ra, còn nhiều học thuyết về liên kết hóa học như thuyết cơ lượng tử, thuyết electron… hầu hết các học thuyết, thuật ngữ đều nói đến các loại liên kết trong hóa học nằm trong các dạng sau:
Các liên kết hóa học thường gặp
Liên kết hóa học được giảng dạy trong nhà trường với một số học thuyết khá phổ biến. Theo Thuyết tĩnh điện của Kossel (1888-1967) về liên kết ion là: chuyển electron hóa trị từ nguyên tử này sang nguyên tử khác, nguyên tử mất “e” chuyển thành Ion dương, nguyên tử nhận “e” tạo thành Ion “âm”, các Ion ngược dấu thì hút nhau. Vì liên kết ion tương đối bền, nên các chất có liên kết ion thì có điểm nóng chảy cao, ở trạng thái lỏng hoặc nóng chảy thì dễ dẫn điện còn ở thể rắn thì không dẫn điện, chúng thường không có màu, tồn tại ở thể rắn và dễ vỡ.
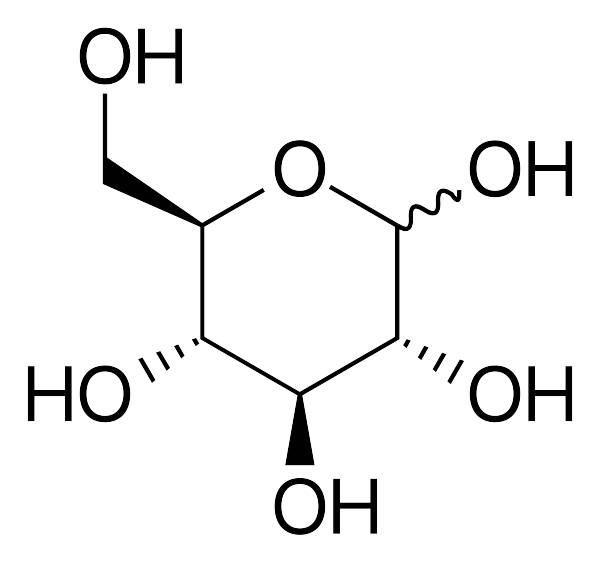
Liên kết hóa học theo Thuyết Lewis nói về liên kết cộng hóa trị: nguyên tử tương tác góp chung một số cặp “e” để tạo thành cặp “e” dùng chung cho 2 nguyên tử. Tại sao? Vì mọi nguyên tử đều hướng tới sự cân bằng (đạt được 2e hoặc 8e ở lớp ngoài cùng) trong nguyên tử). Chình vì vậy mà từ đó hình thành các loại liên kết cộng hóa trị khác nhau: liên kết đơn (có 1 cặp e dùng chung), liên kết đôi (có 2 cặp e dùng chung), liên kết ba (có 3 cặp e dùng chung), ngoài ra còn 1 dạng nữa là liên kết cho-nhận sẽ được giáo viên trình bày thêm với bạn trong các buổi học.
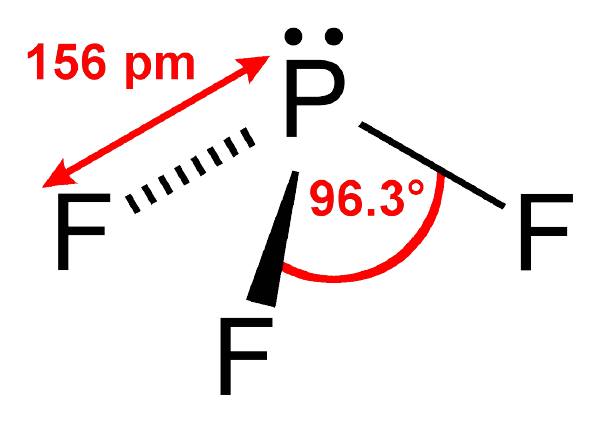
Các liên kết hóa học theo kiểu cộng hóa trị này đều có hướng, có năng lượng liên kết từ 20 – 72kJ/mol khiến các liên kết này khá bền vững, chúng có thể phân cực và không phân cực. Không phân cực nghĩa là liên kết giữa các nguyên tử nguyên tố có độ âm điện bằng nhau, do đó các cặp electron dùng chung không bị nghiêng về bất cứ bên nào, còn liên kết phân cực thì do các nguyên tử nguyên tố có độ âm điện chênh lệch nhau, khiến cho cặp e dùng chung bị nghiêng về một phía (nghiêng về nguyên tử nào có độ âm điện lớn hơn). Các liên kết cộng hóa trị thường được thấy ở các chất rắn như: đường, lưu huỳnh, sắt, nước, rượu, cacbonic, clo, hidro. Các chất như ancol, etylic, đường… tan nhiều trong dung môi có cực như nước, còn các chất hữu cơ không cực, iot lại không tan trong benzene, cacbon tetraclorua.
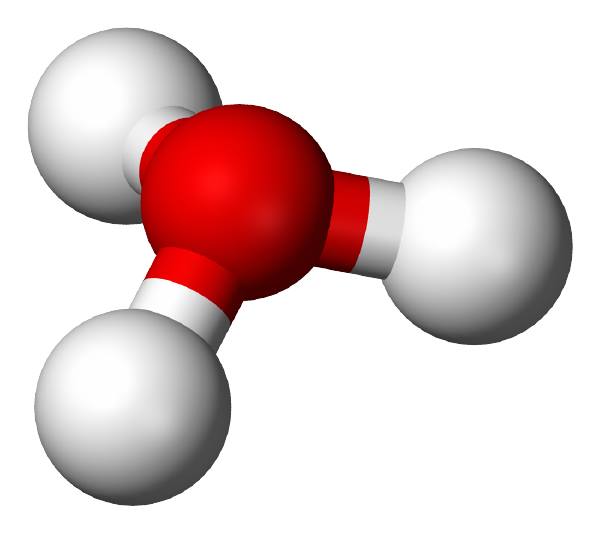
Liên kết hóa học phổ biến khác là liên kết hidro, là liên kết có lực hút tĩnh điện giữa H mang điện dương với các nguyên tố có độ âm điện mạnh, mang điện âm như: N, Cl, O, F… Liên kết Hidro liên phân tử làm tăng nhiệt độ nóng chảy, nhiệt độ sôi, làm giảm độ điện ly của axit, gây biến đổi độ tan (giúp cho chất tan tan tốt hơn trong dung môi nếu nó tạo được liên kết hidro trong đó).
Liên kết hóa học có một số dạng thường gặp như sau. Liên kết ion, liên kết cộng hóa trị, liên kết hidro, ngoài ra, còn có một số dạng khác như liên kết kim loại, liên kết cộng hóa trị phối hợp… nhưng trên đây là 3 loại liên kết phổ biến nhất, thường gặp và hay được vận dụng nhiều nhất để giải các bài tập hóa lớp 10. Nếu các em cần người hỗ trợ kèm riêng tại nhà, hãy liên hệ với chúng tôi để được cung cấp gia sư hóa lớp 10 sẽ giúp các em tìm hiểu thêm về các kiến thức này.